Desde que tenía 14 años, Laura Romero convive con una enfermedad autoinmune: tiroiditis de Hashimoto. Lo que podría haber sido solo un obstáculo en su salud se convirtió en el motor de una carrera científica comprometida con comprender —y modular— los errores del sistema inmunitario. Hoy, tras una trayectoria que la ha llevado por centros punteros como Harvard (EE.UU.) y el Instituto Karolinska (Suecia), esta investigadora posdoctoral se ha especializado en desarrollar estrategias terapéuticas que entrenen al sistema inmune para dejar de atacar al propio cuerpo. Una de ellas, las vacunas tolerogénicas, es el eje de su último estudio, recientemente publicado.
La tiroiditis de Hashimoto es una enfermedad autoinmune que afecta a la glándula tiroides, una pequeña glándula en forma de mariposa situada en el cuello, justo delante de la tráquea. Esta glándula produce hormonas que regulan funciones muy importantes como el metabolismo, la energía, la temperatura corporal o el ritmo cardíaco.
En el caso de Hashimoto, el sistema inmunitario ataca por error a la tiroides, como si fuera una amenaza. Con el tiempo, esto causa inflamación crónica y hace que la tiroides funcione mal, es decir, que produzca menos hormonas de las que debería.
Aunque él no sabía qué causaba la enfermedad, su descripción fue tan precisa que décadas después el neurólogo francés Jean-Martin Charcot, considerado el padre de la neurología moderna, propuso que la enfermedad llevara su nombre en reconocimiento a su aporte.
Un fármaco prometedor contra los daños mitocondriales
A diferencia de las vacunas convencionales, diseñadas para activar al sistema inmune contra patógenos externos, las vacunas tolerogénicas proponen un giro radical: enseñar al sistema inmunitario a tolerar -de ahí proviene el término-, componentes propios del organismo, como el colágeno en las articulaciones afectadas por artritis reumatoide. “La artritis es una enfermedad donde el sistema inmune ataca por error nuestras propias articulaciones. Nuestra vacuna consigue que ese ataque se detenga, sin afectar al resto del sistema inmunológico”, explica Romero. En modelos animales, el resultado fue prometedor: redujo tanto el número de ratones que desarrollaban la enfermedad como la gravedad de los síntomas inflamatorios.
El trabajo, publicado bajo el título “Tolerogenic antigen-specific vaccine induces VISTA-enriched regulatory T cells and protects against arthritis in DRB1∗04:01 mice”, se realizó en ratones humanizados, modificados genéticamente para expresar moléculas inmunológicas humanas. Esto permite que los resultados sean más extrapolables a posibles tratamientos en personas.
Un punto especialmente relevante fue el aumento de expresión de una molécula llamada VISTA, un regulador del sistema inmune. “VISTA actúa como un freno natural ante una respuesta inmunitaria excesiva. Mientras que en la inmunoterapia del cáncer se busca bloquear ciertos mecanismos para potenciar la acción del sistema inmune, en las enfermedades autoinmunes lo que buscamos es precisamente activarla para detener ese ataque”, explica.
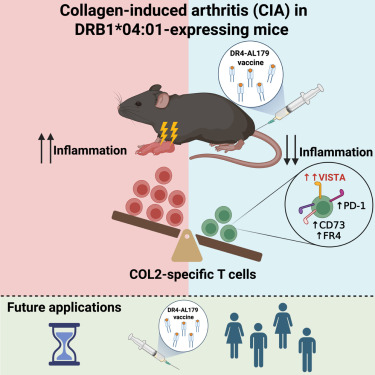
Esta figura resume de manera muy visual lo que Romero consigue con su vacuna tolerogénica. Parte de ratones humanizados, es decir, modificados para tener moléculas inmunológicas humanas, a los que inducen artritis de forma experimental. Como se observa en la imagen, el ratón tiene rayos amarillos que representan la inflamación en las articulaciones. Después del tratamiento con la vacuna, se generan células T específicas -las verdes- que expresan más VISTA, esa molécula que actúa como freno natural del sistema inmune. Estas células consiguen frenar el ataque autoinmune contra las articulaciones de forma muy específica. El resultado no es otro que la reducción drástica de la inflamación. «Lo más prometedor es que esta estrategia podría traducirse en tratamientos para personas con artritis reumatoide: en lugar de suprimir todo el sistema inmunológico, como ocurre en los tratamientos actuales, entrenaremos específicamente a nuestras defensas para que dejen de atacar nuestras propias articulaciones», nos cuenta.
De fosfodendrímeros a checkpoints intestinales
La línea de investigación de Laura Romero ha estado guiada por un objetivo constante: modular la respuesta inmune con precisión. Ya en su tesis doctoral trabajó con fosfodendrímeros —estructuras ramificadas capaces de reducir inflamación sin necesidad de fármacos—, y más tarde, en Suecia, se centró en vacunas tolerogénicas. Ambas estrategias, aunque distintas, comparten una filosofía común: frenar el ataque inmunitario sin desactivar por completo las defensas del organismo. “Lo importante es hacerlo de forma específica, sin suprimir todo el sistema inmunológico como hacen los tratamientos actuales, que aumentan el riesgo de infecciones”, señala.
Estas investigaciones le han valido la dirección de varios proyectos financiados en etapas posdoctorales, algo poco frecuente, y que implica una gran responsabilidad. “Cada año debes demostrar que puedes financiar no solo tu línea de investigación, sino también tu salario. Es estresante, sobre todo si tienes estudiantes a tu cargo, pero también es una etapa de gran crecimiento personal y científico”.
Vuelta a casa, con el intestino en el punto de mira
Tras su etapa internacional, Romero decidió volver a España, esta vez a nuestro Instituto, mediante un contrato postdoctoral senior por la Universidad de Valladolid en el laboratorio Mucosal Immunology Lab. Su actual proyecto posdoctoral se centra en estudiar el papel de VISTA en otra enfermedad autoinmune: la enfermedad inflamatoria intestinal (EII).
Sus primeros datos ya son reveladores. “Observamos que VISTA está muy elevada en el intestino inflamado de pacientes con EII, pero no en sangre. Eso indica que su función podría estar muy localizada, lo que la convierte en una posible diana terapéutica específica”, adelanta. La idea es entender por qué se sobreexpresa, qué la regula y si su modulación podría frenar la inflamación sin efectos sistémicos.

Ciencia con vocación pedagógica y social
Más allá del laboratorio, Romero ha impartido docencia en contextos muy diversos, tanto en España como en el extranjero. “Me adapto más al perfil del estudiante que al país. No es lo mismo explicar inmunología a médicos que a farmacéuticos o bioquímicos”, comenta. También es activa en divulgación científica, participando en eventos como Pint of Science, convencida de que explicar la ciencia a la sociedad es parte del trabajo de una investigadora. “La investigación cuesta dinero y muchas veces los resultados no son inmediatos. Es clave que la gente entienda por qué merece la pena invertir en ciencia”. A las jóvenes investigadoras que empiezan en biomedicina o farmacología les lanza un mensaje claro: mantener viva la pasión. “Sé que es un camino duro, pero si no pierdes la ilusión por lo que haces, siempre habrá razones para seguir adelante”, finaliza.